製品・サービス
目次
DDS用試薬
タンパク質や抗体、siRNAなど様々なバイオ医薬が薬として持つ大きな強みは、その特異性により副作用が少ないことにあります。Iris Biotech社がご提供するアミノ酸をモノマーとするポリマーを用いたドラッグデリバリーでは抗体やペプチドのみでなく低分子を結合することも可能であり、また同じキャリアに複数の有効成分を付与させることができ、症例に合った多剤併用療法を実施することが可能になります。
バイオ医薬品の市場動向と展望
図1.最初期に発売されたPEG化インターフェロン
イギリスのreportbuyer.comの発表によると、全世界でのバイオ医薬の市場規模は2013年時点で2000億ドルにも上るとされ、さらに年率13.5%の成長を続け2020年までに5000億ドルにもなるとも言われています。
一口にバイオ医薬といっても様々な製品が日夜研究、開発されていますが、その中でも抗体医薬は2013年時点で510億ドルの市場を持ち、市場の25.6%を占めています。また、バイオ医薬の適用疾患を領域別に見ると神経精神疾患に関連するものが28.2%を占め、563億円の市場を持ち、これはさらに2020年までに1450億円規模の市場になると予測されています。
タンパク質や抗体、siRNAなど様々なバイオ医薬が薬として持つ大きな強みは、その特異性により副作用が少ないことにあります。通常、それぞれが狙ったターゲットのみに働き、余計な影響を体に与えることがありません。しかしながら、薬物動態特性に改善の必要があることがネックになっています。
そこで、ポリアミノ酸やポリエチレングリコール (PEG) のような生体適合性を持つポリマーを付与(「ポリマー医薬」)することで、バイオアベイラビリティを高め、化学的安定化も可能になると期待されています。現在、これらの物質を付与することによって薬物動態にどのような影響を与えるかという研究が盛んにおこなわれています。
また、もう一つのバイオ医薬の致命的な欠点として免疫系の攻撃を受け、分解、排除されてしまうことがあげられます。これまでに薬物動態特性を向上させる様々な取り組みがなされ、その中でも効果を上げると考えられているのがポリマー医薬です。
一例を挙げると、疎水性が高くかつ生分解性を持つPLA(ポリ乳酸)やPLGA(乳酸とグリコール酸の共重合体)とPEGを組み合わせることによって、生体内の防御機構から薬物を保護する精緻なミセルを形成することができます。
PEGは様々な分野においてもっともよく用いられるポリマーの一つで、ポリマーベースのドラッグデリバリーにも欠かせない物質です。PEG化された化合物が市販されるようになって20年あまりが経過し、様々な臨床的な利点と欠点に関する知見がもたらされてきました。
欠点の一つとしてPEGが分解および代謝されないことにより、体内に蓄積し液胞を形成することによる影響があり、これは詳細に検討することが必要です(下図2)。
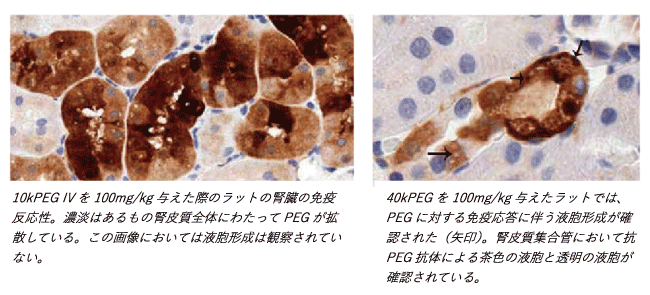
図2.PEGが代謝されないことによる悪影響の例
また近年では、ポリアミノ酸(アルギニン、グルタミン、オルニチンおよびサルコシン) を用いたり、PAS化を利用する方法が研究されています。これらのポリマーはPEGと比べて生体内での分解性に優れ、より高い生体適合性を誇ります。
また側鎖に官能基を持つアミノ酸をモノマーとするポリマーを用いたドラッグデリバリーでは抗体やペプチドのみでなく低分子を結合することも可能であり、また同じキャリアに複数の有効成分を付与させることができ、症例に合った多剤併用療法を実施することが可能になります。
たとえば2014年現在、環状RGD(アルギニン-グリシン-アスパラギン酸)ペプチドとPaclitaxelをPGA(ポリグルタミン酸)に付加させたものは臨床試験フェーズ3の段階にあります。参考文献
ポリマー医薬の基礎と原理
医薬品にポリマーを付加することの意義については、別ページにまとめております。
詳細はこちら
ポリマーの化学的・物理的性質の基礎
ポリマーは通常の低分子とは化学的・物理的にも異なる性質を示します。基礎知識を簡単に別ページにまとめております。
詳細はこちら
PEGに代わる修飾ポリマー
2014年、アメリカでの売り上げTop10の医薬品のうち、多発性硬化症に用いるCopaxone(Glatiramer酢酸塩、Teva社、37億円)およびNeulasta(PEG化したFilgrastim、Amgen社、36億円)医薬品二つがランクインしていることからも、ポリマーを用いた医薬はナノ医薬の先駆者といえるでしょう。
前述の通り、PEGは様々な分野で用いられるポリマーですが、薬学の分野での利用が深まっていく中で、さらなる利便性が見出されるとともに、使用に際して注意すべきことも知見として得られてきています:
▶ PEG自体が副作用を起こしうる。合成過程の副生成物による過敏症も無視できない。
▶ PEGを付与した際に薬物動態特性が予想を超えて変化する場合がある。
▶ PEGは生分解性を持たない。
▶ PEGの分子量を大きくしようとすればするほど、分子量のばらつきの影響が無視できなくなり、医薬品(単一化合物)としての同定や、不純物の除去が難しくなる。
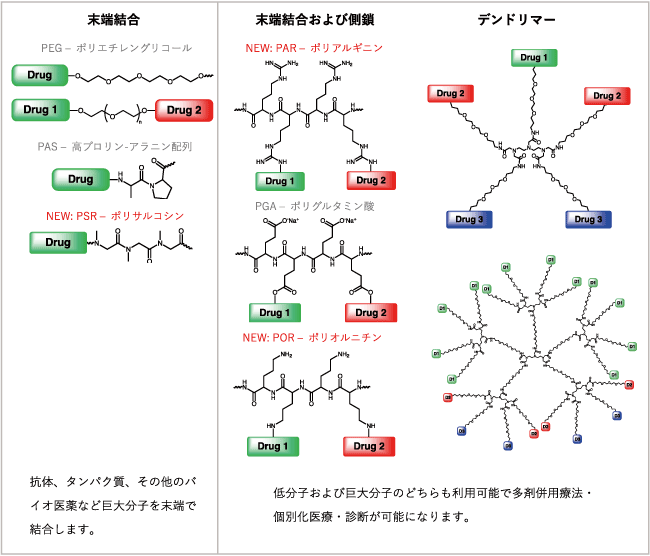
図3.各ポリマーの末端の活用方法参考文献
Iris Biotech社でご提供可能なDDS用ポリマー試薬
Iris Biotech社では、ポリアミノ酸を筆頭に、PEG、ペントリマーなどのDDSにお使いいただける試薬をご提供しております。
PAS化:遺伝子組み換えによる新たな手法
遺伝子組み換えによる新たな手法のご紹介です。分子量分散を持たないポリマーを付与することが可能です。
詳細はこちら
ポリアミノ酸: バイオ医薬品及び低分子医薬に幅広く応用可能な分子
総説はこちら
ポリアルギニン
詳細はこちら
ポリグルタミン酸
詳細はこちら
ポリオルニチン
詳細はこちら
ポリサルコシン
詳細はこちら
ポリエチレングリコール:ポリマー研究の先駆け
総説はこちら
分岐型PEG化試薬
詳細はこちら
アミノ基とカルボン酸を末端に持つPEG(NH2-PEG-COOH)と活性エステル
詳細はこちら
その他の末端修飾された活性化PEG
詳細はこちら
末端にアミン、ヒドラジン、およびグアニジンを持つPEG
詳細はこちら
クリック反応用アルキン-PEG及びアジド-PEG
詳細はこちら
ビオチン-PEG
詳細はこちら
チオール-PEG
詳細はこちら
マレイミド-PEG
詳細はこちら
シラン-PEG
詳細はこちら
その他のPEG関連試薬
詳細はこちら
ペントリマー:5分岐PEGを第一世代とするデンドリマー
詳細はこちら
参考文献
▷ High Molecular Weight Polyethylene Glycol Cellular Distribution and PEG-associated Cytoplasmic Vacuolation Is Molecular Weight Dependent and Does Not Require Conjugation to Proteins; D. G. Rudmann, J. T. Alston, J. C. Hanson and S. Heidel; Toxicologic Pathology 2013; 41: 970-983. doi:10.1177⁄0192623312474726
▷ Poly(ethylene glycol)-Prodrug Conjugates: Concept, Design, and Applications; S. S. Banerjee, N. Aher, R. Patil and J. Khandare; J Drug Deliv. 2012; 2012: 17. doi:10.1155/2012/103973
▷ Poly(ethylene glycol) in Drug Delivery: Pros and Cons as Well as Potential Alternatives; K. Knop, R. Hoogenboom, D. Fischer and U. S. Schubert; Angew Chem. Int. Ed. 2010; 49: 6288-6308. doi:10.1002/ anie.200902672
▷ Integrin-assisted drug delivery of nano-scaled polymer therapeutics bearing paclitaxel; A. Eldar-Boock, K. Miller, J. Sanchis, R. Lupu, M.J. Vicent and R. Satchi-Fainaro; Biomaterials 2011; 32: 3862-3874. doi:10.1016/j.biomaterials.2011.01.073
▷ Molecular assembly composed of a dendrimer template and block polypeptides through stereocomplex formation; H. Matsui, M. Ueda, A. Makino and S. Kimura; Chem Commun 2012; 48: 6181-6183. doi:10.1039/c2cc30926b
▷ Factors Influencing in Vivo Disposition of Polymeric Micelles on Multiple Administrations; E. Hara, M. Ueda, A. Makino, I. Hara, E. Ozeki and S. Kimura; ACS Med Chem Lett. 2014; 5: 873-877. doi:10.1021/ml500112u
▷ Suppressive immune response of poly-(sarcosine) chains in peptide- nanosheets in contrast to polymeric micelles; E. Hara, M. Ueda, C. J. Kim, A. Makino, I. Hara, E. Ozeki and S. Kimura; J Pept Sci 2014; 20: 570-577. doi:10.1002/psc.2655
▷ Thermoresponsive release from poly(Glu(OMe))-block-poly(Sar) microcapsules with surface-grafting of poly(N-isopropylacrylamide);T. Kidchob, S. Kimura and Y. Imanishi; J Control Release 1998; 50: 205-214. doi:10.1016/S0168-3659(97)00135-1
▷ Amphiphilic poly(Ala)-b-poly(Sar) microspheres loaded with hydrophobic drug; T. Kidchob, S. Kimura and Y. Imanishi; J Control Release 1998; 51: 241-248. doi:10.1016/S0168-3659(97)00176-4
▷ On the biodegradability of polyethylene glycol, polypeptoids and poly(2-oxazoline)s; J. Ulbricht, R. Jordan and R. Luxenhofer; Biomaterials 2014; 35: 4848-4861. doi:10.1016/j. biomaterials.2014.02.029
▷ Polypeptoids: A perfect match for molecular definition and macromolecular engineering?; R. Luxenhofer, C. Fetsch and A. Grossmann; J. Polym. Sci.: Part A: Polym. Chem. 2013; 51: 2731-2752. doi:10.1002/pola.26687
▷ Peptide-Based Polymer Therapeutics; A. Duro-Castano, I. Conejos- Sánchez and M. Vicent; Polymers 2014; 6: 515-551. doi:10.3390/ polym6020515
▷ Do HPMA copolymer conjugates have a future as clinically useful nanomedicines? A critical overview of current status and future opportunities; R. Duncan and M. J. Vicent; Adv Drug Deliv Rev 2010; 62: 272-282.doi:10.1016/j.addr.2009.12.005
▷ Polymer therapeutics: Top 10 selling pharmaceuticals — What next?; R. Duncan; J Control Release 2014; 190: 371-380. doi:10.1016/j. jconrel.2014.05.001
